Т»ЎўРнҝЙКВПоЈә
¶юАаУРФҙЎўОЮФҙЎ¶ТҪБЖЖчРөЧўІбЦӨЎ·РнҝЙКВПоұдёь
¶юЎўРРХюРнҝЙДЪИЭ
РнҝЙКВПоұдёьөДКЬАнј°ЙуЕъ
ИэЎў·Ё¶ЁТАҫЭЈә
ЎЎЎЎ1ЎўЎ¶ТҪБЖЖчРөја¶Ҫ№ЬАнМхАэЎ·ЈЁ№ъОсФәБоЁҗөЪ650әЕЈ©
ЎЎЎЎ2ЎўЎ¶ТҪБЖЖчРөЧўІб№ЬАн°м·ЁЎ·ЈЁ№ъјТКіЖ·Т©Ж·ја¶Ҫ№ЬЎшАнЧЬҫЦБоөЪ4әЕЈ©
ЛДЎўЙкЗлМхјю
ЈЁТ»Ј©әУЎҪұұКЎКіЖ·Т©Ж·ја¶Ҫ№ЬАнҫЦәЛ·ўөД¶юАаТҪБЖЖчРөҰ· ЧўІбЦӨЈ¬ЧўІбЦӨј°ЖдёҪјюФШГчөДДЪИЭ·ўЙъұд»ҜЎЈ
ЈЁ¶юЈ©ЙкЗл·ыәПЎ¶ТҪБЖЖчРөЧўІб№ЬАн°м·ЁЎ·ТӘЗуЎЈ
ЈЁИэЈ©ІъЖ·ГыіЖЎўРНәЕЎў№жёсЎўҪб№№ј°ЧйіЙЎўККУГ·¶О§ЎўІъЖ·јјКхТӘЗу·ўЙъұд»ҜөДЈ¬ЧўІбИЛУҰөұПтФӯЧўІбІҝГЕЙкЗлРнҝЙКВПоұдёьЎЈ
ОеЎўЙкұЁЧКБПДҝВјј°ЛөГч
ЈЁТ»Ј©ЙкЗлұн
ЈЁ¶юЈ©ЦӨГчРФЎчОДјю
ҫіДЪЧўЎыІбИЛУҰөұМбҪ»Јә
1.ЖуТөУӘТөЦҙХХёұұҫёҙУЎјюЎЈ
2.ЧйЦҜ»ъ№№ҙъВлЦӨёҙУЎјюЎЈ
ЈЁИэЈ©ЙкЗлИЛ№ШУЪұдёьЗйҝцөДЙщГч
ЈЁЛДЈ©ФӯТҪБЖЖчРөЧўІбЦӨј°ЖдёҪјюёҙУЎЎҝјюЎўАъҙОТҪБЖЖчЁиРөЧўІбұдёьОДјюЎшёҙУЎјю
ЈЁОеЈ©ұдёьЙкЗлПоДҝ¶ФұИұнј°ЛөГч
ёщҫЭҫЯМеұдёьЗйҝцСЎФсМбҪ»ТФПВОДјюЈә
1.ІъЖ·ГыіЖұд»ҜөД¶ФұИұнј°ЛөГчЈ»
2.ІъЖ·јјКхТӘЗуұд»ҜөД¶ФұИұнј°ЛөГч;
3.РНәЕЎў№жёсұд»ҜөД¶ФұИЎФұнј°ЛөГч;
4.Ҫб№№ј°ЧйіЙұд»ҜөД¶ФұИұнј°ЛөЎэГч;
5.ІъЖ·ККУГ·¶О§ұд»ҜөД¶ФұИұнј°ЛөГчЈ»
6.ЧўІбЦӨЦРЎ°ЖдЛыДЪИЭЎұұд»ҜөД¶ФұИұнј°ЛөГчЈ»
7.ЖдЛыұд»ҜөДЛөГчЎЈ
ЈЁБщЈ©УлІъЖ·ұд»ҜПа№ШөД°ІИ«·зПХ№ЬАнұЁёж
ЈЁЖЯЈ©ұд»ҜІҝ·Ц¶ФІъЖ·°ІИ«РФЎўУРР§РФУ°ПмЁҺөДЧКБП
·ЦОцІўЛөГчұд»ҜІҝ·Ц¶ФІъЖ·°ІИ«РФЎўУРР§РФөДУ°ПмЈ¬ІўМṩПа№ШөДСРҫҝЧКБПЎЈККУГ·¶О§ұд»ҜөДұШРлМṩБЩҙІЖАјЫЧКБПЎЈ
ЈЁ°ЛЈ©Хл¶ФІъЖ·јјКхТӘЗуұд»ҜІҝ·ЦөДЧўІбјмСйұЁёж
ЈЁҫЕЈ©·ыәПРФЙщГч
1.ЧўІбИЛЎиЙщГчұҫІъЖ··ыәПЎ¶ТҪБЖЖчРөЧўІб№ЬАн°м·ЁЎ·әНПа№Ш·Ё№жТӘЗуЈ»ЙщГчұҫЎцІъЖ··ыәППЦРР№ъјТұкЧјЎўРРТөұкЧјЈ¬ІўМṩ·ыәПұкЧјөДЗеөҘ;
2.ЧўІбИЛЁ|іцҫЯЛщМбҪ»ЧКБПХжКөРФөДЧФОТұЈЦӨЙщГчЎЈ
ЈЁК®Ј©·ІЙкЗлЖуТөЙкұЁІДБПКұЈ¬°мАнИЛФұІ»КЗ·Ё¶ЁҙъұнИЛ»тЖуТөёәФрИЛұҫИЛЈ¬ЖуТөЎцУҰөұМбҪ»Ў¶КЪИЁЎФОҜНРКйЎ·
БщЎўЙкЗлІДБПТ»°гТӘЗу
ёсКҪј°ЖдЛыТӘўЩЗу
1.ЙкЗлІДБПУҰЗеОъЎўХыҪаЈ¬К№УГA4№жёсЦҪХЕҙтУЎЈ»
2.ГҝПоОДјюөЪТ»ТіЧчЎбұкЗ©Ј¬»тУГҙшұкЗ©өДёфТіЦҪЁӢ·ЦёфЈ¬Іў°ҙЙкұЁЧКБПДҝВјұкГчПоДҝұаәЕЈ»
3.ГҝПоОДјюҫщУҰјУёЗЖуТө№«ХВЈ»
4.°ҙХХЙкЗлІДБПДҝВјөДЛіРтЧ°¶©іЙІбЈ»
5.°мАнТҪБЖЖчРөЧўЎоІбЙкЗлКВОсөДИЛФұУҰөұКЬЙкЗлИЛОҜНРЈ¬УҰіцКҫКЪИЁОҜНРКйј°ёГ°мАнЁyИЛЙн·ЭЦӨГчФӯјюУлёҙУЎјюЎЈ
ЖЯЎўЙкЗлұнёсј°ОДјюПВФШ
1ЎўЧўІбЙкЗлұн.doc
2ЎўТҪБЖЖчРөЧўІбЙкЈАұЁЧКБПТӘЗуј°ЛөГч.doc
3ЎўТҪБЖЖчРө°ІИ«УРЎјР§»щұҫТӘЗуЗеөҘ.doc
4ЎўКЪИЁОҜНРКйЈЁІОҝјСщКҪЈ©.doc
5ЎўЎ¶№ШУЪ·ўІјТҪБЖЖчРөІъЖ·јјКхТӘЗуұаРҙЦёөјФӯФтөДНЁёжЎ·.doc
6ЎўЎ¶№ШУЪҪшТ»ІҪЧцәГТҪБЖЖчРөІъЖ··ЦАаҪзЎт¶Ё№ӨЧчөДНЁЦӘЎ·.doc
7ЎўЎ¶№ШУЪУЎ·ўҙҙРВТҪБЖЖчРөМШұрЙуЕъіМРтЈЁКФРРЈ©өДНЁЦӘЎ·.docx
8ЎўГвУЪЎСҪшРРБЩҙІКФСйөДөЪ¶юАаТҪБЖЖчРөДҝВјЈЁНЁёж2014ДкөЪ12әЕёҪјюЈ©.doc
9ЎўКөК©Ў¶ТҪБЖЖчРөЧўІб№ЬАн°м·ЁЎ·әНЎ¶МеНвХп¶ПКФјБЧўІб№ЬАн°м·ЁЎ·УР№ШКВПоөДНЁЦӘ.doc
°ЛЎўРРХюРнҝЙЙкЗлКЬАн»ъ№Ш
әУұұКЎКіЖ·ЎэТ©Ж·ја¶Ҫ№ЬАнҫЦ
КЬАнөШөгЈәКҜјТЧҜКРәмЖмҙуҪЦ391әЕРРХюРнҝЙҙуМь
КЬАнКұјдЈәГҝЦЬТ»ЦБЦЬОеЎхЙПОз8Јә30ЎӘ12Јә00Ј¬ПВОз13Јә30ЎӘ17Јә30ЈЁ¶¬Ј©
ГҝЦЬТ»ЦБЦЬОеЙПОзЁҸ8Јә30ЎӘ12Јә00Ј¬ПВОз14Јә00ЎӘ17Јә30ЈЁПДЈ©
ҫЕЎўРРЎвХюРнҝЙҫц¶Ё»ъ№Ш
әУұұКЎКіЖ·Т©Ж·ја¶Ҫ№ЬАнҫЦ
К®ЎўРРХюРнҝЙіМРт
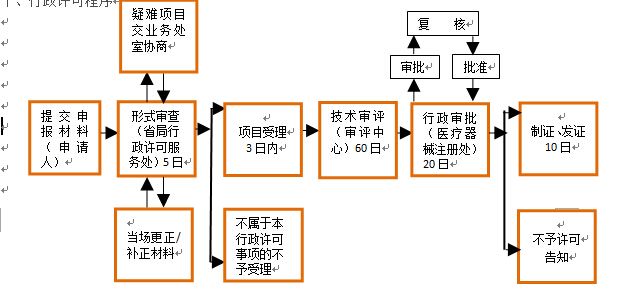
К®Т»ЎўРРХюРнҝЙКұПЮ
1.РнҝЙКВПоұдўЩёьЧФКЬАнЦ®ИХЖр3ёц№ӨЧчИХДЪЧӘҪ»јјКхЙуЖА»ъ№№Ј¬60ёц№ӨЧчИХДЪНкіЙјјКхЙуЖА№ӨЧчЈ¬јјКхЙуЎнЖАҪбКшәу20ёц№ӨЧчИХДЪЧчіцЙу©–Еъҫц¶ЁЁиЎЈЧФЧчіцЙуЕъҫц¶ЁЦ®ИХЖр10ёц№ӨЧчИХДЪ·ўЎМёшТҪБЖЖчРөЧўІбұдёьОДјюЎЈ
2.ЧЁјТЙуЖАЎўЙкЗлИЛІ№ідЧКБПөДКұјдІ»јЖЛгФЪЙуЖАКұПЮДЪЎЈ
К®¶юЎўРРХюРнҝЙЦӨјюј°УРР§ЖЪПЮ
РРХюРнҝЙЦӨјюЈәТҪБЖЖчРөЧўІбұдёьОДјюЎЈ
ТҪБЖЖчРөЧўІбұдёьОДјюУлФӯТҪБЖЖчРөЧўІбЦӨәПІўК№УГЈ¬ЖдУРР§ЖЪУлёГЧўІбЦӨПаН¬ЎЈИЎөГЧўІбұдёьОДјюәуЎэЈ¬ЧўІбИЛУҰөұёщҫЭұдёьЎсДЪИЭЧФРРРЮёДІъЖ·јјКхТӘЗуЎўЛөГчКйәНұкЗ©ЎбЎЈ
К®ИэЎўРРХюРнҝЙКХ·СЈә°ҙУР№ШІҝГЕЕъЎәЧјКХ·С
К®ЛДЎўЧЙСҜ
әУұұКЎКіЖ·Т©Ж·ја¶Ҫ№ЬАнҫЦРРХюРнҝЙ·юОсҙҰөз»°Ў»Јә031183721140
әУұұКЎКіЖ·Т©Ж·ја¶ҪЎҪ№ЬАнҫЦТҪБЖЖчРөја№ЬҙҰөз»°Јә031183720076
ЎЎЎЎЎЎЧўЈәТФЙПЖЪПЮТФ№ӨЧчИХјЖЛгЈ¬І»ә¬·Ё¶ЁЁҗҪЪјЩИХ